Allergy丨周玉峰/钱莉玲团队揭示了环状RNA在儿童哮喘中的调控新机制
哮喘是儿童最常见的慢性呼吸道疾病,近年来,其发病率呈快速上升的趋势,国内1990-2010年儿童哮喘的发病率从1.09%增至3.02%,20年增加了2.8倍。目前上海市儿童的哮喘发病率已超过8%,成为国内发病率最高的城市,严重影响着儿童的生长发育及身心健康。哮喘是一种是由遗传、环境和表观遗传学因素等相互作用而引起的一种免疫炎症性疾病。表观遗传学是不依赖于DNA序列变化而由染色质改变产生的可稳定遗传的表型,包括DNA甲基化、组蛋白修饰、RNA修饰、非编码RNA等。
非编码RNA是指不能编码蛋白质的RNA,包括miRNA,长链非编码RNA(LncRNA)和环状RNA(circRNA)等。既往认为非编码RNA是一群垃圾RNA,最近研究发现非编码具有重要的免疫调节功能。近年来,周玉峰课题组围绕表观遗传学因素和非编码RNA在哮喘及过敏性疾病中的调控作用进行了大量研究工作,取得了系列成果:发现了miRNA(miR-511-3p)(JACI,2018,PMID: 28629744)、长链非编码RNA(LncRNA PTPRE-AS1)和组蛋白甲基化修饰(Science Advances,2019,PMID: 31844669)、长链非编码RNA Lnc-BAZ2B 和乙酰化修饰(JACI,2021,PMID:32712329)和环状RNA Hsa_circ_0004287 和 m6A 修饰(JACI,2022,PMID:34953789)在哮喘和过敏性疾病的诊断和治疗中的作用及机制。
2022年9月14日,我院周玉峰团队和复旦大学附属儿科医院钱莉玲课题组在世界过敏领域TOP期刊《过敏科学》(Allergy)杂志在线发表题为circS100A11 enhances M2a macrophage activation and lunginflammation in children with asthma的文章,揭示了环状RNA在调控M2型巨噬细胞活化及儿童过敏性哮喘中的作用和机制。

该研究通过基因芯片分析发现在儿童哮喘患者外周血单核细胞中有372个差异表达的环状RNA,其中circS100A11的表达明显升高。功能研究发现circS100A11能促进M2型巨噬细胞活化:在巨噬细胞中敲低circS100A11的表达可显著抑制M2型巨噬细胞相关基因CD206,CD209的表达;而过表达circS100A11则促进M2型巨噬细胞活化相关基因的表达。在机制研究方面发现:circS100A11可竞争结合细胞周期相关蛋白1(CAPRIN1),解除CAPRIN1对S100A11的蛋白翻译的抑制,进而促进S100A11的蛋白表达。而S100A11可竞争结合核仁素(nucleolin)而促进转录因子SP3的释放,游离的SP3可结合在STAT6转录起始点上游-1300bp处,促进信号传导及转录激活蛋白6(STAT6)的表达从而促进巨噬细胞M2活化,增强Th2细胞趋化因子CCL17和CCL22的表达。在体内过表达circS100A11,可增强蟑螂提取物诱发的过敏性哮喘小鼠的哮喘症状;而敲低S100a11则能够减轻哮喘小鼠的哮喘症状。既往全基因组关联分析(GWAS)研究显示,S100a11与哮喘相关,但机制不清,本研究也首次阐明了S100a11通过调控M2巨噬细胞活化,参与哮喘发生和发展的分子机制。
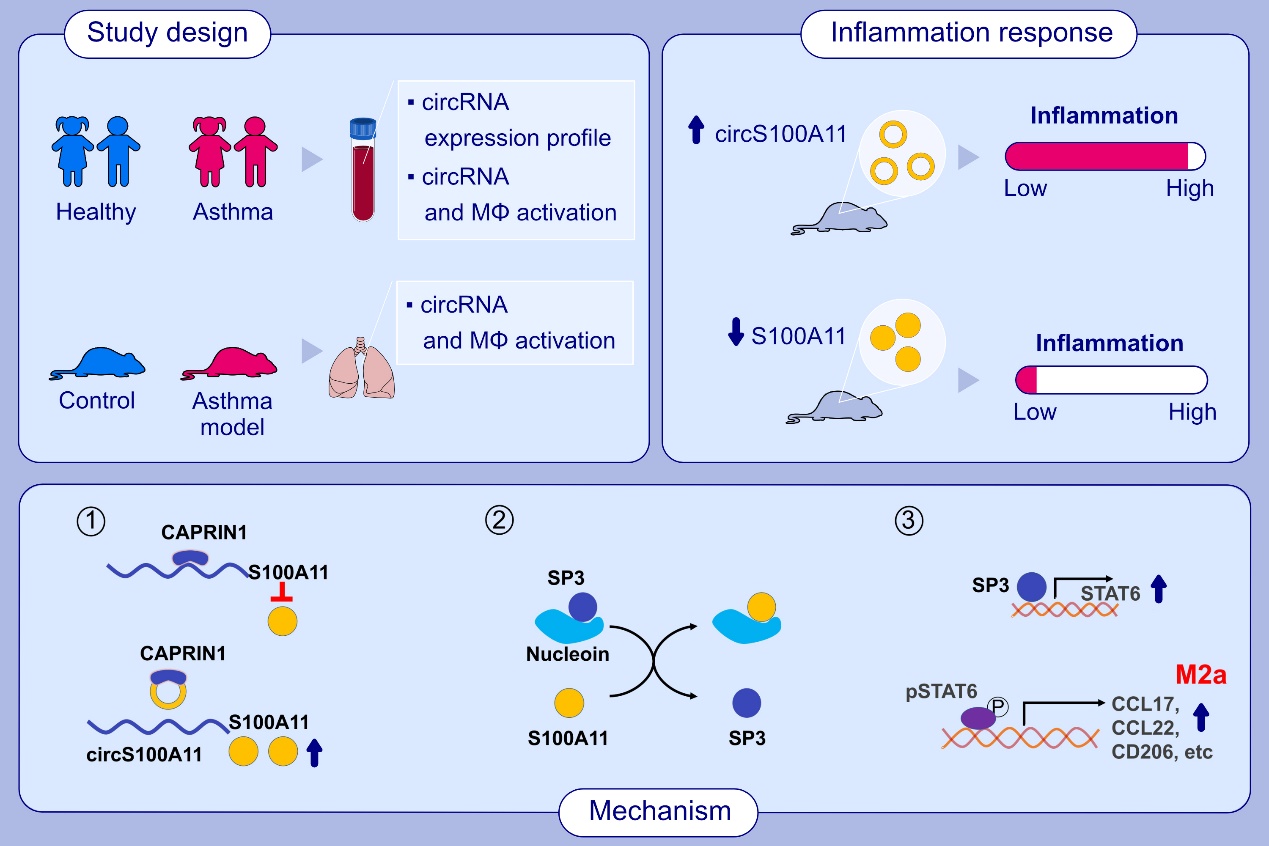
综上,该研究提示circS100A11能促进巨噬细胞M2活化而加重哮喘。circS100A11通过竞争结合CAPRIN1而促进S100A11的表达。S100A11通过竞争结合nucleolin释放出的转录因子SP3,促进SP3与STAT6启动子区域的结合,从而促进STAT6的表达和巨噬细胞M2活化。体内及体外实验表明circS100A11及S100A11在加重哮喘疾病的过程中发挥重要作用,可成为哮喘患儿潜在的诊断及治疗靶标。
据悉,复旦大学附属儿科医院博士研究生梁秋妍和付劲蓉主治医师为文章的共同第一作者;复旦大学附属儿科医院/生物医学研究院周玉峰研究员和附属儿科医院钱莉玲研究员为文章的共同通讯作者。
原文链接: https://onlinelibrary.wiley.com/doi/10.1111/all.15515
DOI:https://doi.org/10.1111/all.15515