Cell Discovery丨陈振国/孙蕾团队与合作者报道利用非奥密克戎中和抗体构建广谱抗新冠奥密克戎和沙贝病毒的双特异中和抗体
新冠奥密克戎突变株自2021年11月发现后,传播迅速,一个月内就成为了世界主要流行毒株,目前已进化出许多分支亚型,比如BA.2, BA4, BA.5等。由于奥密克戎突变株及其亚型对大多数新冠病毒中和抗体,包括许多处于临床阶段的中和抗体药物,产生免疫逃逸,因此,亟需开发出对奥密克戎突变株及其亚型具有广谱中和活性的抗体药物。
2022年10月7日,我院陈振国研究员、孙蕾研究员与复旦大学黄竞荷研究员、上海市免疫治疗创新研究院吴凡研究员、广州医科大学附属第一医院赵金存教授合作在Cell Discovery上发表题为“Combating the SARS-CoV-2 Omicron (BA.1) and BA.2 with potent bispecific antibodies engineered from non-Omicron neutralizing antibodies”的研究论文。该研究利用非奥密克戎中和抗体构建出一系列双特异性广谱中和抗体,通过协同诱导奥密克戎刺突蛋白形成“双三聚体”(Trimer dimer)结构的机制,广谱抑制包括奥密克戎BA.1、BA.2在内的多种新冠VOCs、SARS-CoV和其他沙贝病毒。

首先,研究团队利用从新冠康复患者体内鉴定出3株新冠病毒强效中和抗体GW01、16L9、4L12,他们均能中和新冠Alpha, Beta, Gamma, 以及Delta突变株,其中广谱中和抗体GW01还能中和SARS-CoV以及蝙蝠冠状病毒(WIVI、Rs3367)(Cell Discovery 2022),竞争结合实验显示GW01与16L9、4L12在新冠病毒包膜刺突蛋白上的结合表位也不一致。然而,由于奥密克戎突变株在这些抗体的主要中和表位上发生免疫逃逸,单独使用这些抗体或者抗体组合均不能有效中和奥密克戎突变株。
为了解决这个问题,研究团队利用GW01、16L9、4L12、以及已报道的强效中和抗体REGN10987作为亲本抗体,将抗体的scFv,用linker相连,然后融合构建到IgG Fc构建表达了10株单基因编码的IgG样双特异性中和抗体,令人惊喜的是,8株双特异中和抗体与奥密克戎突变株的刺突蛋白三聚体和RBD有着非常强的结合力与亲和力,而且这8株双特异性中和抗体均能强效中和包括奥密克戎BA.1、BA.2在内的新冠VOC(几何平均(GM)IC50值最低为4.5 ng/mL)。此外,6株双特异性中和抗体对SARS-CoV和蝙蝠SARS相关冠状病毒也具有很强的中和活性(GM IC50最低为11.6 ng/mL)。这些结果显示,将非奥密克戎中和抗体构建为双特异性中和抗体,可产生协同作用,与简单的抗体组合相比能更有效应对病毒突变,是一种优于“抗体鸡尾酒疗法”的治疗策略。

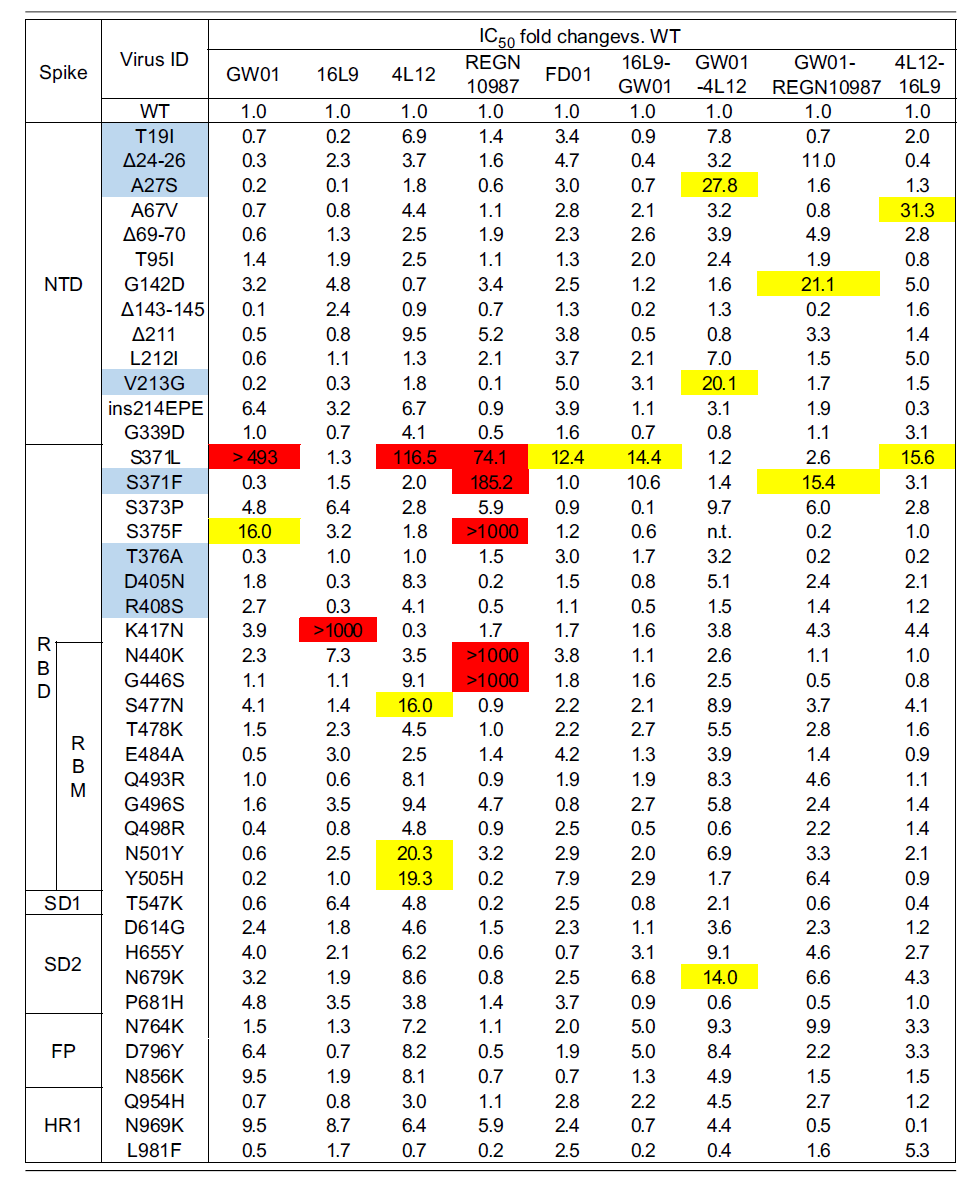
为进一步研究双特异性抗体中和奥密克戎突变株的分子机制,研究团队构建了42个奥密克戎BA.1、BA.2包膜刺突蛋白上所有单点突变假病毒株,比较了GW01、4L12、16L9、REGN10987和双特异性抗体对单点突变毒株的中和活性,实验结果显示,双特异性广谱中和抗体能耐受奥密克戎S371F/P、S375F、K417N、N440K和G446S等关键逃逸突变,从而呈现出广谱且强效的中和活性。
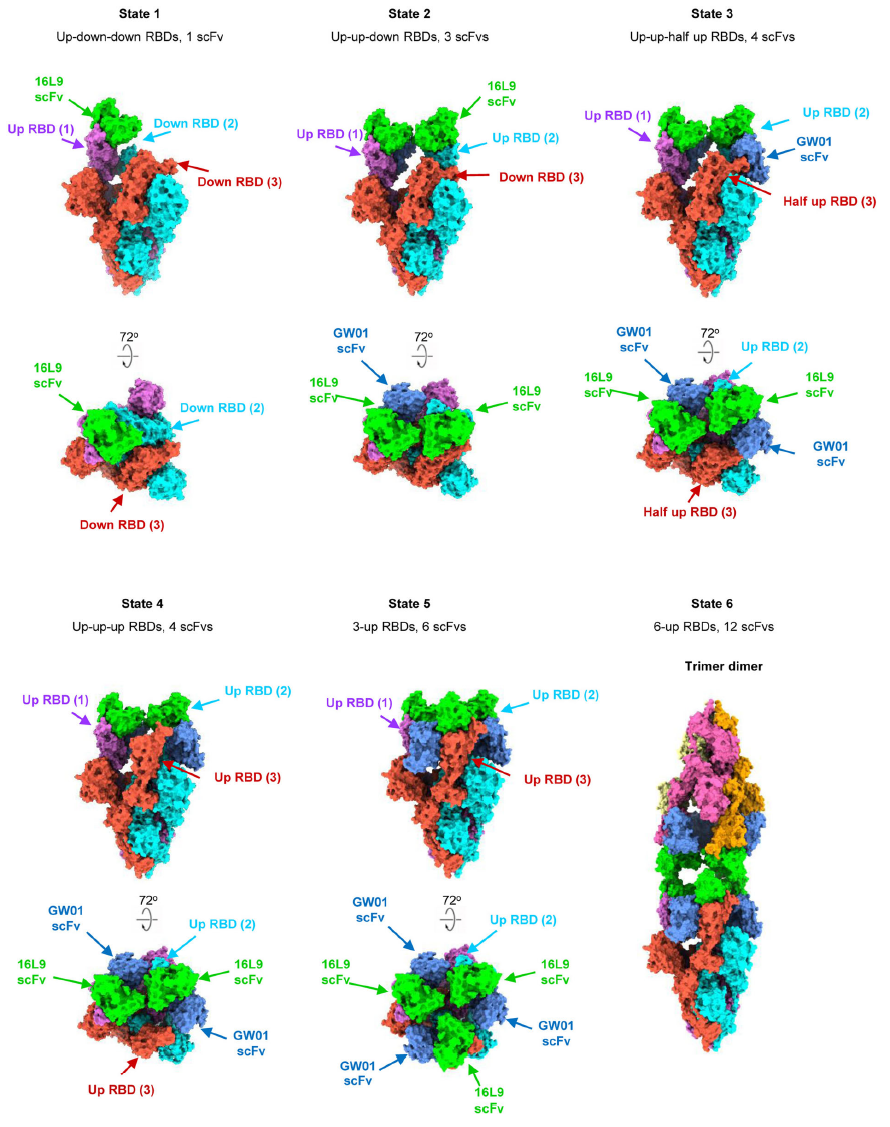
研究团队进一步利用冷冻电镜技术解析了双特异性抗体FD01(GW01-16L9)与奥密克戎刺突蛋白三聚体结合的高分辨率三维结构。研究发现,FD01与奥密克戎刺突蛋白三聚体结合后呈现6种不同的构象,包括一种特殊的“双三聚体”结构。首先,16L9 scFv-GW01 scFv与三聚体的“up”RBD顶端结合后,会诱发旁边的“down”RBD变成“up”RBD;然后,当第2个16L9 scFv-GW01 scFv再结合到第2个“up”RBD后,会再诱发第3个“down”RBD变成“up”RBD,如此类推。最终,三个FD01 IgG分子同时结合两个不同的三聚体,诱导“双三聚体”的形成,双三聚体上的6个RBD全部处于“up”状态,从而抑制包膜刺突蛋白上RBD与ACE2蛋白的结合。虽然16L9、GW01单克隆抗体不能与奥密克戎包膜刺突蛋白紧密结合,但是以他们为亲本抗体构建的双特异性中和抗体由于结构的特殊性,能促进两个scFv协同作用,增加了抗体结合RBD的表位和亲和力,从而耐受S371L等免疫逃逸突变,抑制奥密克戎突变株BA.1、BA.2假病毒的感染。有趣的是,前不久该研究团队也报道了一个奥密克戎中和抗体6M6同样能诱导刺突蛋白产生“双三聚体”结构,从而抑制病毒感染(Cell Research 2022)。因此,利用奥密克戎非中和抗体构建的双特异性抗体也能通过协同作用诱导刺突蛋白产生类似结构而达到广谱中和效果。
综上所述,本项研究报道了基于非奥密克戎中和抗体构建的双特异性广谱中和抗体具有协同作用,促进奥密克戎刺突蛋白形成“双三聚体”结构,揭示了一种全新的双特异性中和抗体抑制病毒感染的机制,为设计广谱抗奥密克戎和沙贝病毒的中和抗体药物研发提供了新思路。
复旦大学基础医学院医学分子病毒重点实验室、上海市重大传染病和生物安全研究院、上海市公共卫生临床中心黄竞荷研究员,上海市重大传染病和生物安全研究院、复旦大学附属第五人民医院、复旦大学生物医学研究院陈振国研究员、孙蕾研究员,上海交通大学医学院附属仁济医院/上海市免疫治疗创新研究院吴凡研究员,广州医科大学附属第一医院赵金存教授为该研究的共同通讯作者。复旦大学王应丹、张翔、马云萍,广州医科大学王延群为该研究的共同第一作者。该研究得到了上海市科技重大专项、国家自然科学基金、国家科技部、国家科技重大专项、上海市卫生健康委、中国医学科学院、复旦大学附属上海第五人民医院人才计划经费支持。
原文链接:
https://www.nature.com/articles/s41421-022-00463-6