Leukemia丨石玉衡/周丹/高海合作报道 STING通路在介导DNMT3A突变克隆性造血进展过程中的功能研究
克隆性造血 (Clonal hematopoiesis, CH) 是造血干细胞由于基因突变而引起的干细胞克隆扩增,并伴随下游谱系异常分化的血液发育现象。目前研究证明CH的发生发展与白血病发生以及衰老相关疾病的进展,如心肌梗死,慢性肺梗阻,阿尔兹海默症等,表现出了高度相关性。DNMT3A是一种从头 DNA 甲基转移酶,参与调控基因组胞嘧啶甲基化修饰稳态。在CH样本中,DNMT3A突变是最常见的遗传事件,发生率高达40-50%,小鼠模型证明缺失Dnmt3a基因会直接导致CH的发生,提示了DNA表观修饰异常是CH发生的直接原因。人群队列分析也指出,在血液肿瘤样本中,DNMT3A突变通常作为“首次打击”事件,与其他基因突变(如 FLT3-ITD、NPM1)协同作用会引发血液肿瘤。但由于表观遗传调控涉及面广,作用时间长,因此 DNMT3A 功能缺失如何导致 CH 的发生以及介导血液疾病恶性转化的具体调控机制和参与关键信号通路目前尚未明晰。
2025年2月22日,复旦大学生物医学研究院青年副研究员石玉衡与合作者在Leukemia杂志上发表了文章题为 “STING mediates increased self-renewal and lineage skewing in DNMT3A-mutated hematopoietic stem/progenitor cells” 的研究论文。该研究首次报道了 cGAS-STING 通路在 Dnmt3a 缺失造血干细胞/祖细胞(Hematopoietic stem/progenitor cells, HSPCs)中的激活机制以及其对HSPC自我更新和下游细胞偏系分化的影响,并证明抑制该信号通路可以有效的缓解 Dnmt3a 缺失诱发CH的进展,并延缓了携带DNMT3A突变血液恶性肿瘤的发展速度。

研究者通过分析野生型和 Dnmt3a缺失小鼠骨髓中不同分化阶段血液细胞的转录组测序数据,发现 cGAS-STING 信号通路在Dnmt3a 缺失的HSPCs 中被激活,下游的炎症因子水平表达显著升高。使用 STING 抑制剂 C-176可以显著抑制 Dnmt3a缺失 HSPCs 的体外集落形成能力。在原位小鼠的表型观察中,敲除 Sting显著减缓了 Dnmt3a 缺失 HSPCs 异常增强的自我更新能力。利用非竞争移植模型和竞争移植给药模型,研究者证明了抑制或敲除 Sting能显著抑制 Dnmt3a缺失 HSPCs 向髓系细胞分化的倾向以及异常的扩增,从而抑制 Dnmt3a 缺失导致的 CH 的发生发展。
机制上,研究者发现,Dnmt3a缺失导致 ERVs 的去甲基化是激活 cGAS-STING 通路激活的关键机制(而不是传统认为的DNA损伤)。通过全基因组甲基化测序和RNA-seq分析,研究者发现 Dnmt3a缺失的 HSPCs 中 ERVs 基因区域的甲基化水平显著降低,而 ERVs 的表达显著升高,ERVs 逆转录形成的 cDNA 是导致HSPC中 STING 通路的激活的信号分子。抑制 ERVs 的逆转录过程可以有效抑制 Dnmt3a缺失 HSPCs 的体外集落形成能力和体内自我更新能力。
同时,研究者在携带 Dnmt3a和 Flt3 共突变的AML小鼠模型以及 DNMT3A突变患者来源的异种移植模型中验证了 STING抑制剂在治疗白血病中的疗效,发现 STING抑制剂可以显著延缓白血病的进展,并延长小鼠的生存期。
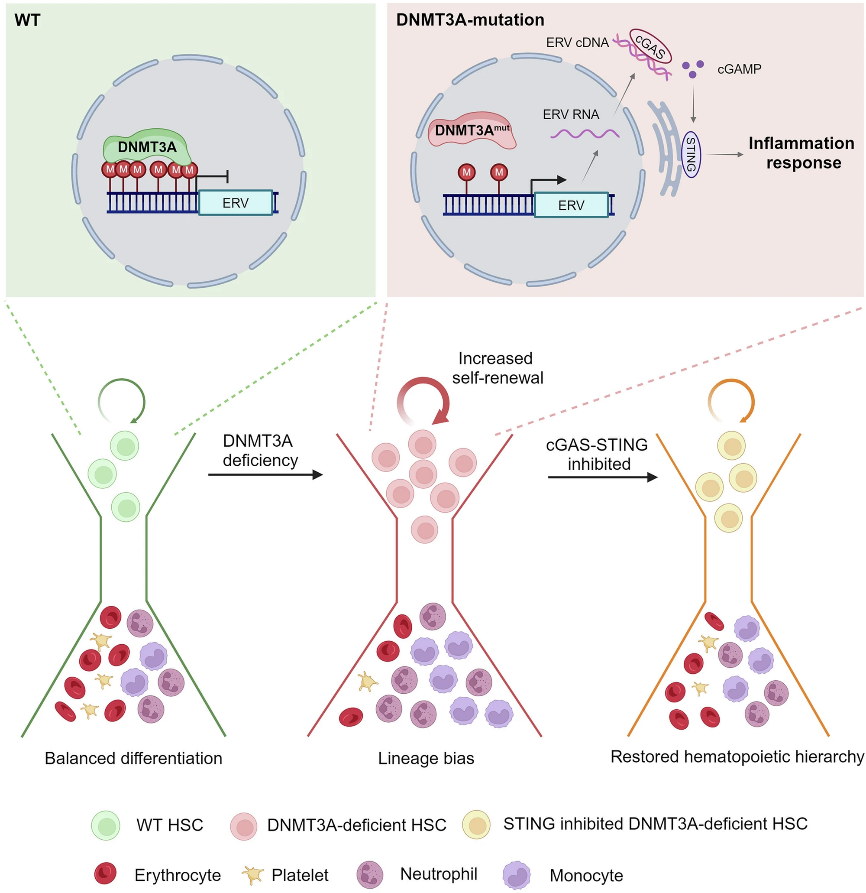
本研究提出了 STING通路在 DNMT3A 突变 HSPCs 中的激活机制,并揭示了其在自我更新和偏系分化中的关键作用,证实了 DNMT3A 缺失导致的内源性慢性炎症对 CH 以及血液系统恶性肿瘤发生发展的重要推动作用。该研究不仅为 DNMT3A 功能缺失导致 CH 的发生以及向恶性血液疾病转化的具体调控机制提供了新的见解,还为预防和治疗DNMT3A突变相关的血液疾病提供了新的方向。
复旦大学生物医学研究院博士研究生黄静茹、谢佳颖博士(已毕业,现就职于仁济医院)、博士研究生王吟为论文的共同第一作者。石玉衡青年副研究员,周丹青年副研究员,高海青年研究员为本文共同通讯作者,以上在组人员均为徐国良院士团队成员。值得一提的是,本研究是石玉衡青年副研究员与团队合作者围绕STING分子在CH发生以及白血病靶点开发领域的第3篇研究工作,前期2篇研究工作也同样发表于Leukemia杂志,分别介绍了STING在TET2突变CH中的具体作用以及在AML1-ETO白血病中作为潜在靶点的可行性。结合本研究工作,研究团队通过一个系列文章,论证了STING作为CH的早期干预靶点的可行性,相信未来会有更多的研究对相关的实际应用做出探索。本项目由国家自然科学基金委,科技部重点研发计划,中国医学科学院创新单元,复旦大学血液病精准医学研究中心-华山医院,复旦大学中山-徐汇中心医院提供相关经费支持。
全文链接:https://www.nature.com/articles/s41375-025-02542-5