Journal for ImmunoTherapy of Cancer丨罗敏/卢智刚团队报道瘤内注射激活STING的纳米疫苗提高抗肿瘤免疫效果
整合含有天然免疫刺激分子的纳米制剂、以及个性化新抗原筛选技术,使肿瘤疫苗在临床测试展现了令人瞩目的有效性【1】。新一代的肿瘤疫苗与CAR技术﹑免疫检查点干预成为免疫治疗中重要的三大板块。然而,在很多病人中,T细胞无法通过肿瘤屏障进入瘤内,导致对多种免疫治疗的不敏感;因此促进T细胞进入肿瘤,逆转肿瘤微环境成为提高免疫治疗效果的重要步骤【1,2】。
2022年5月27日,我院罗敏/卢智刚团队和德克萨斯大学西南医学中心高金明团队合作,在Journal for ImmunoTherapy of Cancer发表“Intratumoral Administration of STING-Activating Nanovaccine Enhances T Cell Immunotherapy”论文。该研究发现,和传统的皮下注射疫苗(S.C.)相比,利用目前临床可行的瘤内注射技术进行疫苗免疫(I.T.),能够在瘤内形成髓系细胞/CXCL9-T细胞/IFNγ正反馈循环,显著促进T细胞向肿瘤募集,从而优化了肿瘤微环境,并对远端转移肿瘤也产生更为有效的治疗效果。这一研究结果为肿瘤纳米疫苗的应用提供了新的治疗方式,并为无法手术或术后原位免疫清除的癌症病人提供了免疫治疗新策略。

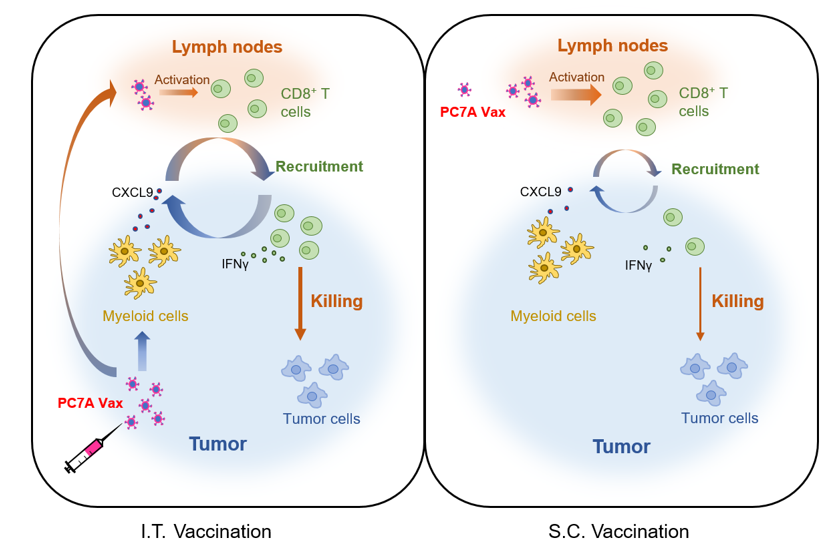
该团队所开发的肿瘤纳米疫苗由聚合分子PC7A和抗原肽组成;~30nm的粒径使其能够被主动递送到淋巴结,并利用其激活STING通路的特性和PH响应性促进抗原交叉呈递,显著刺激肿瘤特异性T细胞的活化,具有广泛有效的抗肿瘤效果【3】。基于这款疫苗,该团队比较皮下注射和瘤内注射的免疫效果,发现在多种肿瘤模型中,瘤内注射纳米疫苗显示出更为有效的抗肿瘤效果。
机制分析表明,该抑瘤效果由CD8+T细胞所介导。瘤内免疫纳米疫苗促进外周T细胞向肿瘤迁移,显著增加了肿瘤中抗原特异性的CD8+T细胞的含量。进一步研究发现,瘤内注射方式中,纳米疫苗一方面能够主动递送到肿瘤同侧的引流淋巴结、诱导肿瘤特异性T细胞的活化;同时驻留在瘤内的疫苗能够刺激髓系细胞产生CXCL9,招募外周T细胞进入肿瘤;而这些T细胞产生的IFNγ进一步刺激瘤内髓系细胞产生更多的CXCL9,从而形成一个髓系细胞/CXCL9-CD8+T/ IFNγ正向循环,导致肿瘤中效应T细胞的进一步增强。
临床上肿瘤转移是造成治疗效果差和死亡的重要原因。该研究利用双侧荷瘤的小鼠模型以及肺转移模型,进一步证明原位肿瘤的瘤内免疫,对远端肿瘤及肺转移的病灶发展也产生了更为有效和长期的抑制效应。同时,该策略能够与肿瘤特异新抗原有机结合,为个性化肿瘤疫苗的开发提供了新的平台。
复旦大学生物医学研究院罗敏研究员、卢智刚研究员,以及美国德克萨斯大学西南医学中心高金明教授为该论文的共同通讯作者,复旦大学研究生蒋小艺与西南医学研究中心博士后王健为文章共同第一作者。
原文链接:
https://jitc.bmj.com/content/10/5/e003960
参考文献
Galon J, Bruni D. Approaches to treat immune hot, altered and cold tumours with combination immunotherapies. Nat Rev Drug Discov 2019;18(3):197-218. doi: 10.1038/s41573-018-0007-y
Hailemichael Y, Dai ZM, Jaffarzad N, et al. Persistent antigen at vaccination sites induces tumor-specific CD8(+) T cell sequestration, dysfunction and deletion. Nat Med 2013;19(4):465-+. doi: 10.1038/nm.3105
Luo M, Wang H, Wang Z, et al. A STING-activating nanovaccine for cancer immunotherapy. Nat Nanotechnol 2017;12(7):648-54. doi: 10.1038/nnano.2017.52