表观遗传团队在《Science Advances》揭示组蛋白H3.3突变促进肿瘤发生的机制
组蛋白H3是遗传物质的基本单位核小体的主要组成之一,其尾部含有多种组蛋白翻译后修饰,并且参与调控多种生物学过程。近年来,多个科研团队陆续在肿瘤组织中发现组蛋白H3上高频发性“驱动性突变”(Driver mutations)的存在,包括高级别少儿脑瘤中的K27M以及G34R/V突变,软骨细胞瘤中的K36M突变以及骨巨细胞瘤中的G34W/L突变等。
近日,复旦大学生物医学研究院郭睿副研究员与哈佛大学Shi Yang教授、St Jude儿童研究医院Suzanne J. Baker教授等合作,发现并证明了染色质识别蛋白RACK7能够识别组蛋白H3.3G34R突变,并且抑制主要组织特异性抗原复合物(major histocompatibility complex,MHC)II分子的产生以及细胞内转运过程,阐述了组蛋白H3.3G34R突变促进肿瘤发生的一种可能的分子生物学机制。7月17日,相关成果以“RACK7 recognizes H3.3G34R mutation to suppress expression of MHC class II complex components and their delivery pathway in pediatric glioblastoma”为题在线发表于Science Advances杂志上。

H3.3G34R突变主要发生在少儿胶质母细胞瘤(Glioblastoma multiforme ,GBM)病人组织中,世界卫生组织WHO根据肿瘤的恶性程度将脑部肿瘤分为四级,GBM属于恶性程度最高的IV级脑瘤,它是最常见的实体脑瘤之一,五年生存率不足5%。H3.3G34R突变在脑瘤中的作用机制的研究对于GBM的治疗具有重要意义。
研究团队通过体外纯化重组蛋白,发现RACK7可以在体外特异性的识别含有H3.3G34R突变的多肽以及重组核小体。并证明RACK7的PHD结构域是识别H3.3G34R突变的关键结构域。随后,研究团队从少儿胶质母细胞瘤中分离纯化培养得到含有H3.3G34R突变的胶质母细胞瘤细胞系。在两例H3.3G34R细胞系中RACK7均可以结合染色质,而通过CRISPR/Cas9方法将H3.3G34R突变更正为野生型H3.3后,RACK7对染色质的特异性识别显著降低。为了进一步验证RACK7与H3.3G34R的关系,研究团队发现将H3.3G34R更正为H3.3野生型或者敲除RACK7会造成相同基因的表达变化,主要包括MHC II分子,其伴侣蛋白CD74, CIITA以及囊泡相关基因。进一步分析发现是由于在H3.3G34R细胞中RACK7识别MHC II分子的关键调控基因—CIITA和囊泡基因染色质所致。MHC II分子是T细胞调节细胞免疫过程的主要参与分子之一,在抗原提呈细胞、小胶质细胞、神经干细胞等细胞中表达。新生成的MHC II分子在内质网上被组装之后,通过多种囊泡结构,依次转运加工直至插入细胞膜中,被CD4+ T淋巴细胞所识别,并参与免疫反应。该项研究表明RACK7与H3.3G34R突变相互作用影响MHC II分子合成以及细胞内转运的整个过程。
除了抑制MHC II免疫应答过程,研究团队还发现RACK7通过与组蛋白H3.3G34R突变的相互作用,可以在含有H3.3G34R突变的肿瘤细胞中抑制细胞分化相关基因的表达。同时,敲除RACK7或者将H3.3G34R突变更正为野生型均可以降低肿瘤细胞的转移以及侵袭能力。这说明,H3.3G34R招募RACK7可以对少儿胶质母细胞瘤细胞的肿瘤特性产生影响。
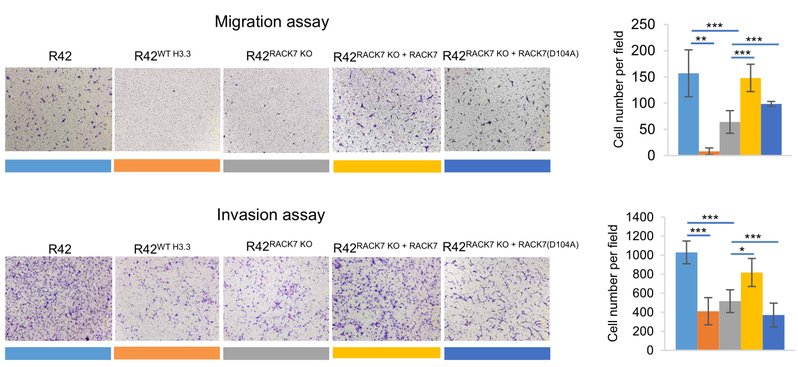
RACK7敲除和将H3.3G34R突变为H3.3能够抑制细胞转移和侵袭
综上所述,该研究鉴定到组蛋白驱动性突变H3.3G34R的识别子RACK7,并且在肿瘤组织中分离纯化得到的H3.3G34R细胞系中证明该相互作用。该研究首次指出RACK7在H3.3G34R的细胞中抑制MHC Class II体系免疫应答,维持H3.3G34R细胞的肿瘤特征。RACK7可能成为含有H3.3G34R突变的这一类胶质母细胞瘤的治疗靶点。
据悉,该项研究第一作者为复旦大学生物医学研究院焦芳芳博士、李泽副研究员和郭睿副研究员,郭睿副研究员同时也是论文通讯作者。H3.3G34R少儿胶质母细胞瘤细胞系由St Jude儿童研究医院Suzanne J. Baker教授课题组Chen He博士纯化分离完成。
原文链接:https://advances.sciencemag.org/content/6/29/eaba2113