复旦温文玉组揭示HECT型E3连接酶的一种多锁酶活调控机制
泛素连接酶E3选择特异靶蛋白和位点,因而决定了泛素化修饰的特异性。HECT型E3在多种生理过程中发挥重要作用,包括细胞周期进程、细胞增殖、自噬和炎症,其调节异常与癌症、免疫紊乱和神经系统病变等人类疾病密切相关,作为潜在的治疗靶标引起了广泛关注。HECT型E3的C端含有特征的由N/C两个lobe组成的HECT结构域,能够接受从E2转移的泛素并随后将泛素转移至特定底物。基于不同的N端结构域,HECT型E3可分为几个亚家族,其中最大的家族Nedd4有9个成员(WWP1 / 2,Nedd4 / 4L,Smurf1 / 2,NEDL1 / 2和Itch),其N端由一个负责亚细胞定位的C2结构域和2-4个负责底物识别的WW结构域组成。
为了防止底物和自身过度泛素化,HECT型E3通常利用分子内或分子间相互作用来抑制自身的活性。近期,Philip A. Cole组(Mol Cell, 2017)与温文玉组(EMBO Rep, 2017;JBC, 2018)分别报道了WWP2、Itch及其果蝇同源蛋白Su(dx)的自抑制机制,结果表明WW2结构域及随后的一段Linker(L)通过占据HECT上的泛素结合位点及限制C-lobe的自由度来抑制它们的活性。这种WW2L介导的自抑制可以通过WW结构域结合含多个PY motif的接头蛋白Ndfip1、或JNK1介导的磷酸化、或者L的磷酸化来释放。然而许多问题仍然存在,如HECT类E3是否存在共同的调节机制?WW2L是否参与调控其他Nedd4家族成员的活性?HECT结构域是否存在其他的调控位点?
2019年7月18日,复旦大学生物医学研究院/华山医院神经外科温文玉课题组在Nature Communicaitons杂志上发表了题为“A multi-lock inhibitory mechanism for fine-tuning enzymeactivities of the HECT family E3 ligases”的研究工作,该研究揭示了Nedd4家族E3普遍采用一种可变的多锁抑酶活性调控机制,拓展了对HECT类泛素连接酶活性调控的认识。

该研究解析了WWP1在完全抑制状态(2L34HECT)和部分激活状态(L34HECT)的晶体结构(下图)。结构分析表明,WW2,L和WW4形成类似头戴式耳机的结构,其中WW2和WW4结合在HECT N-Lobe的两侧,而L形成α-螺旋结合在HECT的N-和C-lobe之间。WWP1的WW2L结合HECT的模式与WWP2/Itch非常相似。有趣的是,HECT的N端延伸序列占据了WW4结构域中的经典PY motif结合位点。这种多位点相互作用通过阻止E2-E3的泛素转移过程使WWP1保持在完全无活性状态,而WWP1众多癌症相关的突变使其转为半开放的构象从而增强了WWP1连接酶活性,并可能通过增加ΔNp63α泛素化降解来促进肿瘤细胞迁移。
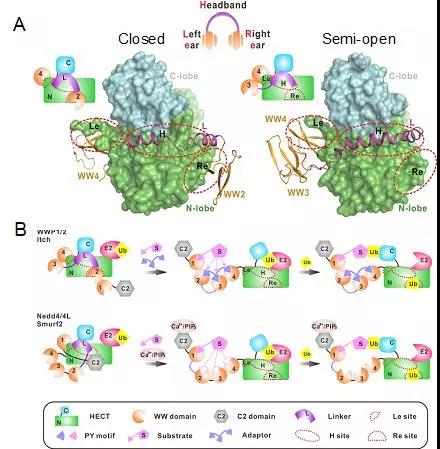
最后,研究表明这种多锁调节机制在WWP2和Itch中是保守的,而Nedd4/4L和Smurf2使用略有不同的多锁抑制机制。总体而言,该研究揭示了HECT家族泛素连接酶多样的调控机制。除了先前报道的“Re”和“H”位点,它们分别负责结合WW2(WWP2和Itch)或C2(Smurf2和Nedd4 / 4L)和L(WWP2和Itch),该研究发现了HECT上一个新的“Le”调控位点。通过“Re”/“H”或“Le”/“H”双位点结合,Nedd4 E3可以保持部分激活状态;当“Re”,“H”和“Le”位点全部被占据时(即多锁调控),Nedd4 E3处于完全自抑制状态。这种多层调节机制可以使Nedd4 E3表现出不同的活性,从而更精确地调控细胞的各种生理进程。在这些调节位点处的翻译后修饰或激动剂的结合可以使这些E3处于部分或完全活性状态。然而,这些位点的病理性突变则会引起E3酶活性的错误调节从而导致许多疾病,如癌症。该研究为理解这些病理性突变提供了可能的分子机制。
温文玉题组的王振和刘子亨博士为该论文的共同第一作者;温文玉研究员为该论文的通讯作者。
原文链接:
https://doi.org/10.1038/s41467-019-11224-7