EMBO J | 余发星团队揭示Hippo信号通路分子新架构及功能调控新理论
Hippo信号通路在器官尺寸调控、组织再生和肿瘤发生等过程中发挥关键作用,自发现以来一直受到广泛的关注,是理想的药物靶点【1】。明确该通路的分子架构和调控机制是开发相应治疗策略的基础。
Hippo通路通常被认为是一个“线性”的激酶级联反应:MST1/2激酶/MAP4Ks激酶–LATS1/2激酶–YAP/TAZ转录共激活因子【2】。但是,在小鼠肝脏中敲除Hippo通路不同基因导致截然不同的器官尺寸和肿瘤类型【3,4】,这些遗传学数据很难用现有的“线性” 信号转导模型来解释。因此,为了深入理解LATS1/2和YAP/TAZ如何整合上游信号并发挥生物学功能,有必要重新审视Hippo信号通路的分子架构。
2023年3月15日,复旦大学生物医学研究院/附属儿科医院余发星团队在The EMBO Journal杂志以长文形式发表了题为Two Hippo signaling modules orchestrate liver size and tumorigenesis的研究论文。该研究重构了Hippo通路核心信号网络,首次提出HPO1和HPO2“双模块”信号转导模型,二者协同调节LATS1/2和YAP/TAZ的活性,决定不同的细胞命运、器官尺寸和肿瘤进程。

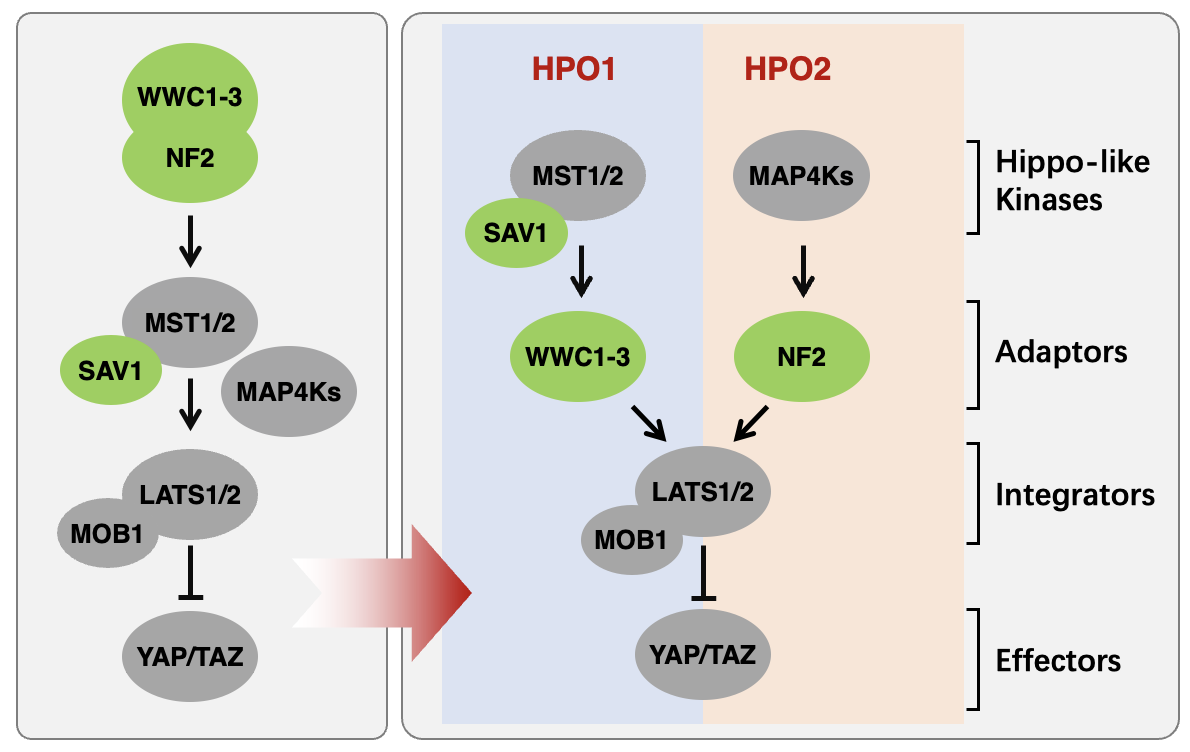
NF2和WWC蛋白在Hippo信号转导过程中发挥重要作用。在本项工作中,研究人员发现,在NF2和WWC蛋白缺失细胞和组织中,LATS1/2激酶活性显著降低,而MST1/2和MAP4Ks的激酶活性则不受影响。进一步研究表明NF2和WWC蛋白能够直接与LATS1/2发生强相互作用。这些发现提示NF2和WWC蛋白在MST1/2和MAP4Ks下游发挥作用,而这与以往研究提出的模型有所不同。研究团队近期报道了WWC蛋白促进LATS1/2磷酸化的机制,这种作用依赖于SAV1和MST1/2,不依赖于NF2和MAP4Ks【5】;另外,NF2是MAP4Ks激酶底物,二者间存在蛋白相互作用【6】。本研究发现NF2可能作为接头蛋白介导MAP4Ks对LATS1/2的磷酸化修饰和活化。基于上述结果,本文提出了Hippo信号通路包括HPO1和HPO2两个信号转导模块,即MST1/2-SAV1-WWC1-3构成的HPO1和MAP4K1-7-NF2构成的HPO2,二者协同调节LATS1/2和YAP/TAZ的活性和功能。该模型在纵向将Hippo通路成员分为四个层次,从上游到下游依次为:Hippo样激酶(MST1/2和MAP4Ks)、接头蛋白(adaptors, 包活WWC蛋白,SAV1和NF2), 整合蛋白(integrators, LATS1/2)和效应蛋白(effectors, YAP/TAZ);同时,在横向将传统的“线性”通路分成两个相对独立的模块HPO1 和HPO2。因此,这一发现从根本上重新构建了Hippo信号通路核心组分的排列架构。
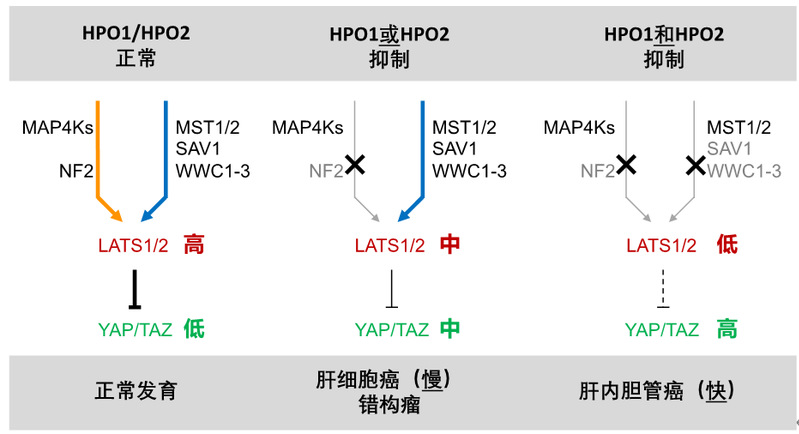
小鼠肝脏尺寸变化和肿瘤发生是Hippo通路功能的经典表型。本研究构建了11种Hippo通路基因(单基因或多基因)肝脏特异性敲除小鼠模型,并对肝脏尺寸和肝脏肿瘤进行了长时程观察。结果显示,HPO1对于器官尺寸调控具有主导作用作用,其完全缺失导致肝脏在2个月内增大4-5倍。在肿瘤发生方面,HPO1或HPO2缺失导致肝细胞癌缓慢发生,相反HPO1和HPO2同时缺失导致肝内胆管癌快速发生。
通过不同基因的组合敲除,研究团队能够灵活构建发病速度不同(1周–15月)、病理等级不同(良性或恶性)、瘤种不同(肝细胞癌或胆管癌)的小鼠肝脏肿瘤模型。因此,HPO1和HPO2在肝脏尺寸和肝脏肿瘤发生方面的功能具有差异性和协同性。
总之,本研究重构了Hippo通路核心信号网络,首次提出Hippo通路“双模块”信号转导模型,并在细胞及小鼠肝脏中进行了严格的检验。该模型在进化上高度保守,能有效地解释在不同Hippo通路基因缺失小鼠或果蝇中观察到的矛盾表型。这些发现为后续Hippo信号通路机制、功能研究和临床转化提供了强有力的理论基础。

(改自网络图片,寓意HPO1/2像两位“门神”,共同守卫Hippo通路的活性)
复旦大学生物医学研究院博士生祁思娴,钟振兴,朱雨闻,王业斌为本文共同第一作者。余发星研究员为通讯作者。中科院分子细胞科学卓越创新中心张雷,麻省大学医学院Mao Junhao及韩国科学技术院Dae-Sik Lim等多位教授对本研究做出了重要贡献。
余发星课题组长期研究Hippo信号通路调控机制及功能(发育及肿瘤),以通讯作者形式在Cell,Molecular Cell,The EMBO Journal,Cell Research,Cell Reports,Protein & Cell,EMBO Reports等期刊发表论文。课题组依托复旦大学生物医学研究院(IBS)和附属儿科医院,研究经费充足,现面向海内外英才,诚聘助理研究员、博士后及实验室管理员,欢迎志同道合、热爱科研的朋友加入,长期有效。详情请见课题组网站http://yu-lab.fudan.edu.cn及IBS官网https://ibs.fudan.edu.cn。
原文链接:https://www.embopress.org/doi/10.15252/embj.2022112126
参考文献:
1. Johnson R, Halder G (2014) The two faces of Hippo: targeting the Hippo pathway for regenerative medicine and cancer treatment. Nat Rev Drug Discov 13: 63-79
2. Yu FX, Zhao B, Guan KL (2015) Hippo Pathway in Organ Size Control, Tissue Homeostasis, and Cancer. Cell 163: 811-28
3. Lu L, Li Y, Kim SM, Bossuyt W, Liu P, Qiu Q, Wang Y, Halder G, Finegold MJ, Lee JS, Johnson RL (2010) Hippo signaling is a potent in vivo growth and tumor suppressor pathway in the mammalian liver. Proc Natl Acad Sci U S A 107: 1437-42
4. Yi J, Lu L, Yanger K, Wang W, Sohn BH, Stanger BZ, Zhang M, Martin JF, Ajani JA, Chen J, Lee JS, Song S, Johnson RL (2016) Large tumor suppressor homologs 1 and 2 regulate mouse liver progenitor cell proliferation and maturation through antagonism of the coactivators YAP and TAZ. Hepatology 64: 1757-1772
5. Qi S, Zhu Y, Liu X, Li P, Wang Y, Zeng Y, Yu A, Wang Y, Sha Z, Zhong Z, Zhu R, Yuan H, Ye D, Huang S, Ling C, Xu Y, Zhou D, Zhang L, Yu FX (2022) WWC proteins mediate LATS1/2 activation by Hippo kinases and imply a tumor suppression strategy. Mol Cell 82: 1850-1864 e7
6. Ma M, Zhong Z, Zhu Y, Gu Y, Jin R, Meng Z, Wang Y, Yu F-X (2022) Phosphorylation of NF2 at Serine-13 by MAP4K family kinases mediates pathological angiogenesis. Protein & Cell