Mol Cell | 雷群英课题组发现新的精氨酸感知通路BAG2-SAMD4B信号轴
营养代谢物质在细胞内如何被感知一直是生物医学领域重要科学问题。精氨酸(L-精氨酸)作为一种条件必需氨基酸,其感知机制异常与癌症、肥胖、癫痫和神经退行性疾病以及衰老过程密切相关。近年来研究发现mTORC1和GCN2是经典的精氨酸感知通路,但细胞是否存在独立于上述经典通路之外新的精氨酸感知机制仍然不清楚。
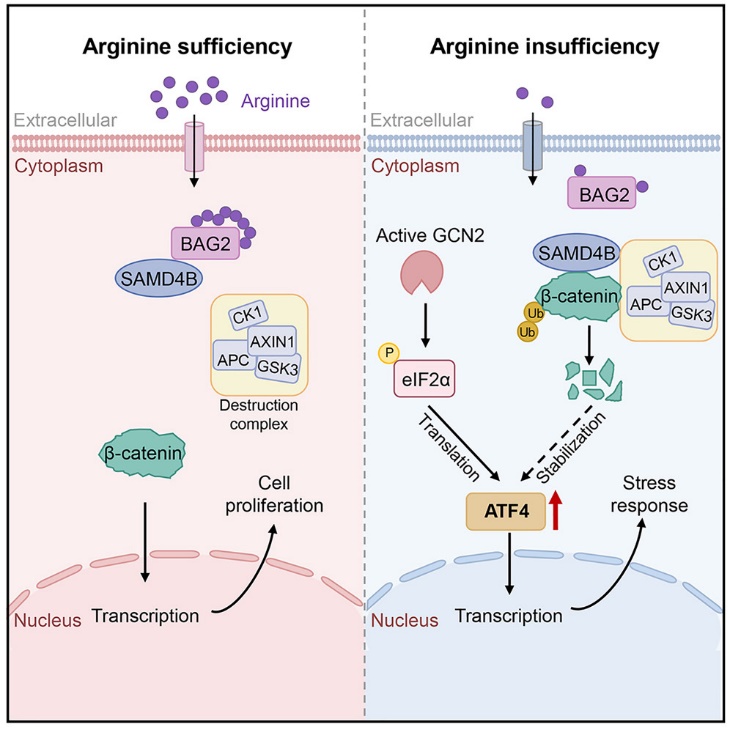
2025年6月23日,生物医学研究院雷群英团队在Molecular Cell上发表论文“BAG2 releases SAMD4B upon sensing of arginine deficiency to promote tumor cell survival”,揭示Bcl-2相关抗凋亡基因2 (BAG2)作为新的精氨酸感知蛋白,响应精氨酸饥饿后,释放不育阿尔法基序结构域蛋白4B(SAMD4B),从而导致β-Catenin蛋白发生降解,进而稳定ATF4蛋白。该信号轴与GCN2–eIF2α通路协同作用,共同调节整合应激反应(ISR),促进肿瘤细胞在精氨酸缺乏条件下的存活。

研究人员通过对哺乳动物肝癌和结直肠癌的研究,首先发现在精氨酸缺乏条件下激活Wnt/β-Catenin会诱导肿瘤细胞凋亡,其依赖于ATF4蛋白的下调。精氨酸缺乏促进β-Catenin的泛素化进而导致其蛋白水平降低,且该感知机制不依赖于经典的mTORC1和GCN2营养感知通路。通过一系列无偏倚高通量筛选策略,研究人员发现BAG2通过其谷氨酰胺残基167(Q167)直接结合精氨酸,当精氨酸充足时,BAG2与SAMD4B之间的结合增强,阻止β-Catenin的降解,从而激活Wnt/β-Catenin信号通路以维持肿瘤细胞存活。当精氨酸缺乏时,BAG2释放SAMD4B,促进β-Catenin发生降解,进而稳定ATF4蛋白,提高肿瘤细胞在低精氨酸条件下的生存能力。
研究人员进一步通过体内实验发现SAMD4B敲除联合精氨酸限制饮食显著抑制小鼠结直肠癌细胞的增殖,表明BAG2-SAMD4B信号轴对于肿瘤细胞在代谢压力下的生存具有重要意义,提示靶向BAG2-SAMD4B轴干预精氨酸感知,联合ADI-PEG20疗法,有望为解决精氨酸限制疗法的耐药提供潜在的新策略。
近年来,雷群英教授团队发现了系列代谢感知和感知异常新信号通路,表明体内存在非mTOR等经典通路依赖的多种代谢感知新通路,证实细胞代谢受到精细的时空调控,突破了经典的细胞代谢感知理论。
复旦大学生物医学研究院孙春雨博士生和复旦大学肿瘤研究所陈梦影博士为论文共同第一作者,复旦大学基础医学院前沿创新中心马齐襄青年副研究员、复旦大学上海医学院雷群英教授和复旦大学附属肿瘤医院尹淼副研究员为共同通讯作者,该研究得到了国家重点研发计划、国家自然科学基金、上海市教育委员会"曙光计划"、上海市市级科技重大专项、新基石科学基金会的支持。
原文链接:https://doi.org/10.1016/j.molcel.2025.05.035